Tag: 新冠疫苗
中国高福院士:我已接种新冠候选疫苗
中国疾病预防控制中心主任高福院士近日表示,他已经注射了一种实验型新冠病毒疫苗,希望通过此举增强公众信心,在疫苗获批后接种。
据美联社报道,高福在由阿里巴巴旗下的阿里健康(Alibaba Health)和美国科学期刊出版商Cell Press于7月26日共同主办的一场网络研讨会上透露上述消息,“我希望它有效。”不过,高福并没有具体提及他何时以及如何接种这种候选疫苗,原因是不想被视作为疫苗生产公司“做宣传”。
高福表示,他注射疫苗是为了增强公众对疫苗的信心。由于多种阴谋论和部分人士对科学家的恶意攻击,很多人对新冠疫苗的作用表示质疑,“作为一名科学家,你必须勇敢。如果连我们都不接种疫苗,我们怎么能说服全世界——所有人去接种疫苗?”
美莫德纳新冠疫苗猴子试验效果良好 每疗程定价310至465元
美国生物科技公司莫德纳(Moderna Inc.)研发的新冠肺炎疫苗mRNA-1273,据报在猴子身上进行试验时效果良好。猴子注射了疫苗后,免疫系统作出积极反应,也能成功阻止在新冠肺炎病毒在鼻子和肺部繁殖。最新消息指出,该公司计划为这种疫苗定价为每一个疗程50至60美元(约390至465港元),较另外两家药厂辉瑞(Pfizer)和德国BioNTech研发的疫苗贵最少11美元(约85港元)。
据英国《金融时报》昨日(28日)报道,莫德纳研发的疫苗定价适用于美国及其他富有国家和地区。该公司的发言人以机密为由,拒绝披露详情,只是说,现时正与不同国家的政府洽商供应疫苗的事宜。
另一名消息人士透露,莫德纳在现阶段仍然未为新疫苗的价格作最后决定。
根据辉瑞和BioNTech与美国政府达成的20亿美元(约155亿港元)协议,每个疗程注射两剂的价格为39美元(约300港元)。按照计划,该两家公司会为美国5000万人供应疫苗。辉瑞、BioNTech和默沙东药厂均表示,计划靠出售疫苗赚取利润。强生集团(Johnson & Johnson)则表示,不打算借此牟利。
辉瑞昨日表明,该公司出售给其他发达国家的疫苗,价格不会比在美国的售价为低。该公司表示,可能需要接受多过一次疫苗,才可发挥保护作用。
辉瑞高层指,预期人们需要继续注射疫苗多年,以维持免疫力,这是因为疫苗的免疫力会日久减弱,而病毒亦可能会变种。
另一方面,根据一篇昨日在《新英格兰医学杂志》刊登的报告,莫德纳研发的新冠肺炎疫苗在猴子身上进行试验时,效果良好,产生大量抗体。猴子的免疫系统产生积极反应,也能阻止那种病毒在鼻子和肺内繁殖。
相比之下,英国牛津大学研发的疫苗在猴子身上进行试验时,并没有得出同样效果。牛津疫苗只是能阻止病毒进入动物的肺部及减轻动物的病情。
在莫德纳进行的试验中,有三批各8只猕猴参与试验,分两剂各10微克及100微克的安慰剂或疫苗,注射入牠们体内。结果显示,所有注射了疫苗的猕猴都产生大量能对抗新冠肺炎病毒的抗体,水平甚至较人类康复者的抗体为高。
牠们注射第二剂疫苗后四周,获安排透过鼻子接触新冠肺炎病毒或利用喉管把病毒打入牠们肺部。两天后,研究人员察觉不到病毒在牠们体内有繁殖的迹象。
中英两款疫苗最有希望 两强PK谁能胜出?
(4月10日,工作人员在国药集团中国生物新冠疫苗生产基地展示新型冠状病毒灭活疫苗样品。图源:新华社)
好消息!7月20日晚,国际学术期刊《柳叶刀》同时在线发布两篇论文,分别介绍了中国和英国两款新冠疫苗的临床试验成果。腺病毒载体疫苗路线上的两个“明星”呈现出“双雄争霸”的态势。
虽然两款疫苗采用了同一研发路线,但从试验设计到试验结果上,二者到底有何异同?中国疫苗的研发特点如何?如何看待牛津疫苗的潜力?
“双剂保护”与“单剂免疫” 怎样更有效?
中国工程院院士、军事科学院军事医学研究院研究员陈薇领衔团队研发的“Ad5腺病毒载体疫苗”,在全球范围内,第一个进入Ⅱ期临床试验,最重要的特点就是纳入了60岁以上的受试者,占508位志愿者总数的13%。
该疫苗生产合作方康希诺生物股份有限公司董事长宇学峰在接受科技日报记者采访时强调:“从设计思路上,二者工作机理相似,都是刺激平衡的体液和细胞免疫,不同之处在于,我们希望在大流行的情况下,单剂免疫即可有效,而牛津团队更进一步测试了‘双剂保护’。”
牛津大学官方网站文章记录了牛津疫苗研究项目首席研究员、研究论文的合著者安德鲁·波拉德教授的观点:“在接受双剂疫苗的10名参与者中,我们看到了(Ⅰ/Ⅱ期临床共1077名18—55岁志愿者中)最强的免疫反应,表明这(双剂疫苗)可能是接种疫苗的好策略。”
这一表述并未获得宇学峰的完全认同。他认为,疫情大流行的趋势下,自然是“一针见效的疫苗起效最快”,现在中国疫苗Ⅱ期临床试验结果显示,在疫苗接种第28天时,高剂量组95%的受试者和低剂量组91%的受试者,均诱发了T细胞免疫反应或抗体免疫反应。
“这说明单剂疫苗不仅起效快,免疫效果也完全能获得保证!”
需要指出的是,与年轻人群相比,年龄较大的受试者对该疫苗的耐受性较好,但免疫反应水平相对较低。
陈薇的观点被媒体广泛采用。一旦感染新冠病毒,老年人将面临严重疾病甚至死亡的高风险。因此,老年人是新冠疫苗的重要目标人群。
宇学峰表示,再加一针强化,会非常有效地增强免疫反应,康希诺采用相同技术研制的埃博拉疫苗临床试验中也证实了两针免疫的效果。未来的临床研究中,也有可能探索对老年人怎样实现更好的保护。
“黑猩猩”与“人” 哪个载体选择更安全?
除了有效性外,两款疫苗的安全性如何?
牛津大学这款AZD1222疫苗,是把来自新冠病毒的遗传物质与已知能导致黑猩猩感染的普通感冒病毒(腺病毒)的弱化版本结合在一起。而据宇学峰介绍,中国“Ad5腺病毒载体疫苗”采用的载体Ad5病毒,是能导致人而非黑猩猩感染的普通腺病毒弱化版本。“虽然部分受试者因此前感染过Ad5病毒而拥有‘既存免疫力’,会影响部分人群的疫苗免疫效果,但从腺病毒载体的源头看,中国疫苗从根本上最大程度地确保了安全性。”
目前,从媒体公开信息观察对“安全性”的描述,两款疫苗“旗鼓相当”:牛津疫苗没有严重的不良事件,疲劳和头痛是最常见的症状,其他常见的副作用包括注射部位疼痛、肌肉疼痛、发冷和发烧;中国疫苗大部分受试者出现的不良反应是轻微或中度的,比如发热、疲劳和注射部位疼痛。
《柳叶刀》同期发表约翰·霍普金斯大学疫苗专家纳尔·巴·泽夫和威廉·摩斯的评论称,尽管在载体选择、人群地理位置和分析方法上有所不同,但这两款腺病毒疫苗结果大致相似且很有希望。不过评论也同时指出,尽管这两项疫苗试验都显示了成功的希望,但试验规模仍然很小,因此应谨慎解读这些结论。
“全球可及”:中英疫苗共同的目标与承诺
据美国消费者新闻与商业频道(CNBC)报道,当地时间7月20日,世界卫生组织应急项目执行主任迈克·瑞安博士在日内瓦总部的新闻发布会上说:“在产生T细胞反应和中和抗体方面,这是一个积极的结果,但还有很长的路要走,我们现在需要进入更大规模的试验。”
瑞安补充道,如果一款疫苗被证明有效,下一个挑战将是确保有足够的剂量在全球分发。
宇学峰表示,康希诺一直是陈薇院士团队和牛津大学团队的战略合作伙伴,在新冠疫苗的最初研发阶段,康希诺选择了前者,“但不可否认,牛津团队与阿斯利康的合作,在下一步的Ⅲ期临床全球试验志愿者征集上,拥有潜在优势”。
虽然牛津疫苗在腺病毒疫苗生产线上的水平仍与康希诺有差距,但其有望借助巨额资助和全球疫苗分发网络的支持获得“加速”,并在疫苗Ⅲ期临床试验结果出来后,实现大规模量产。
来源:科技日报
编辑:刘义阳
审核:朱丽
终审:冷文生
协和大学专家与中港团队合作 疫苗或明年初面世
(■■协和大学与来自中国及香港的国际伙伴共同研发新冠肺炎疫苗。协和大学)
协和大学(Concordia University)与来自中国的大学研究人员、香港伊利沙伯医院等国际伙伴,共同研发新冠肺炎疫苗。研究团队并非在实验室而是留在家里工作,采用崭新电脑及人工智能技术进行测试,可望为全球发明划算的疫苗。
该研究团队使用反向疫苗学,这是一种科学的方法,利用生物信息学和基因组测序,以便分解病毒的结构信息,并且提供合理价格的通用疫苗。协和大学教授兼分子模拟研究中心总监,也是该项目加方研究负责人柏苏哈尔(Gilles Peslherbe)称,由于此研究使用基因建模来解构病毒,因此可以研发具有持久免疫反应的疫苗,而且不受年龄、性别或背景的影响。
与柏苏哈尔一起合作的是赛瓦拉吉(Gurudeeban Selvaraj)和卡利摩西(Satyavani Kaliamurthi),他们两人来自印度,也是中国河南科技大学的研究员。作为米迪斯环球联线计划(Mitacs Globalink Program)的一部分,他们于去年12月抵达满地可,进行为期24星期的实习,与国际学生和当地研究员一同参与该计划。
原研究肺癌 改发展疫苗
两名研究员原定于4月返回中国,因实施新冠肺炎疫情及居家令,米迪斯计划团队安排延长他们在加拿大的居留期限,并将其工作从肺癌和子宫颈癌的研究,转为发展抗新冠肺炎病毒的解决方案。他们与柏苏哈尔定期进行视像会议,又与国际伙伴中国河南科技大学、上海交通大学及香港伊利沙伯医院共同研发疫苗。
加拿大的研究小组正在改进疫苗,中国的合作伙伴则于今年夏季,在实验室为疫苗的动物临床试验做准备。柏苏哈尔表示,如果一切都按计划进行,疫苗可能会在2021年初面世。如果没有米迪斯计划和国际合作伙伴,将无法协调这项研究。因为实习生和合作伙伴带来专业知识,使这个研究迅速发展。
两名研究员的学术背景对研究产生助力,其中卡利摩西对子宫颈癌有研究经验,并且由于她先前的子宫颈乳头状瘤疫苗研究具有相似的性质,这种感染可将子宫颈细胞改变为癌前细胞,因此她能够利用此方法研究疫苗。而赛瓦拉吉先前针对肺癌和呼吸道疾病的新药设计工作,同样加速是次研究的进度。星岛记者报道
英国牛津大学疫苗初步显示有效产生抗体 最快9月面世
英国牛津大学与阿斯利康药厂共同研发的新冠状病毒疫苗,初步显示能够在人体引发免疫反应。研究人员预计9月可生产逾100万剂疫苗,年底前可广泛使用。
这项英国政府有份资助的新冠肺炎疫苗研究,四月开始测试,研究团队公布首阶段测试数据,约一千人自愿接受注射疫苗。
结果显示91%人接种第一剂疫苗后一个月开始产生免疫反应,而接种了两剂疫苗的人全部都有免疫反应,没有引起严重副作用。疫苗令他们产生可以抗击病毒的抗体及白血球。白血球是免疫系统细胞,帮助身体抵抗细菌入侵及其他感染。
不过研究团队表示,现阶段未能确定要接种多少剂量,才能引发足够免疫反应,且仍未能确定疫苗能否避免人体感染新型冠状病毒,甚至减少病征,仍需进行更大型试验,下一阶段会在英国安排超过1万人参与,亦会将试验扩展至其他国家,包括美国、南非及巴西,当中在美国会有3万人参与,以确定疫苗是否有效。研究结果已在医学期刊《刺针》发表。英国政府早前预订100万剂这款疫苗。
报道说今次发现在抗疫方面带来重大曙光,但这款疫苗能否提供充够保护,仍然是言之尚早。
加美英三国联合控诉 俄罗斯试图窃取新冠疫苗研究
一个由俄罗斯支持的黑客组织试图在加拿大、英国和美国窃取与新冠状病毒相关的疫苗研究。
加拿大通讯安全局(CSE)、英国国家网路安全中心(National Cyber Security Centre)、美国国土安全部(DHS)、美国网路安全和基础设施安全局(CISA),与美国国家安全局(NSA)联合发表报告,指出被称为“Cozy Bear”的骇客团体“APT29”试图利用软体漏洞,得到脆弱电脑系统的权限,并且透过“WellMess”、“WellMail”等恶意软体,上传与下载中毒电脑内的资料。他们也利用鱼叉式网路钓鱼,意图诱骗用户交出登入资料。
CSE周四与英国和美国共同发出的声明说,该骇客团体“几乎肯定是作为俄罗斯情报部门的一部分而运作的”。
当被问及恶意攻击是否成功以及针对是针对加拿大哪些设施进行攻击时,一位发言人说,“有关特定网络安全事件的详细信息,CSE无法发表评论或确认”。
声明提到:“这些恶意网络活动很可能会窃取与新冠状疫苗的开发和测试有关的信息和知识产权,并阻碍医疗保健专家和医学研究人员帮助国民的行动。”
自从病毒疫情开始,CSE一直警告,与疫情有关的加拿大知识产权是外国政府资助的骇客入侵之“重要目标”。
CSE在5月份表示,当局正在调查加拿大组织进行与COVID-19相关的研究的可能的安全漏洞,但并未说明攻击背后的人和来源。
俄罗斯克里姆林宫否认涉入骇客行为。
图:CTV
v01
喜讯!美国新冠疫苗实验者全部产生抗体
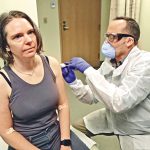
(■西雅图一间研究所三月中给志愿者注射莫德纳公司的疫苗。)
(星岛日报报道)美国生物科技大厂莫德纳公司(Moderna Inc.)和美国国家过敏症和传染病研究所合作研究的新冠肺炎疫苗,第一阶段出现令人鼓舞的试验效果,在受试四十五人身上全都出现抗体反应,且未报告严重不良反应, 即将于本月二十七日展开临牀试验的最后阶段。
莫德纳曾在五月于官网发布第一阶段试验的“初步结果”,显示疫苗在八名患者身上产生免疫反应。而最新结果发表在周二的《新英格兰医学期刊》。这款疫苗是一种信使核糖核酸(mRNA)疫苗,可针对病毒的刺突蛋白发挥作用。刺突蛋白是病毒感染宿主细胞的关键所在,也是过去研发沙士(SARS)冠状病毒疫苗和中东呼吸综合症(MERS)冠状病毒疫苗时的靶点。
三月十六日,这款疫苗的一期临牀试验在位于西雅图的凯撒医疗集团华盛顿卫生研究所启动,四十五名年龄在十八岁至五十五岁之间的健康志愿者参与试验。他们被分为三组,分别接受每次二十五微克、一百微克和二百五十微克剂量的注射,二十八天后注射第二次。 新研究总结了这款疫苗一期临牀试验结果:第一次注射后,三组志愿者都产生了抗体应答,其中二百五十微克剂量组志愿者抗体应答最强;第二次注射后,志愿者体内的抗体滴度都进一步增强。两次注射后,所有志愿者体内均检测到血清中和抗体,且其活性超过对照组的新冠康复者体内的平均水平。
安全性方面,试验结果显示这款疫苗的副作用几乎都是轻度或中度,没有严重不良反应。超过半数志愿者出现疲乏、畏寒、头痛、肌肉痛和接种区域疼痛等症状。第二次接种后副作用更普遍,且接种最高剂量的志愿者副作用更明显。
美国国家过敏症和传染病研究所所长福奇称试验结果为“好消息”,还说研究未发现严重有害结果,且疫苗产生用来杀死/中和病毒的抗体数量“相当高”。没有参与研究的英国卡迪夫大学传染病专家傅利曼说,研究结果显示,这款疫苗“可让身体产生抗体,并随着剂量增加而增加”。他又说,重要的是,在实验室条件下,“身体产生的抗体可以中和病毒”。据美国国家卫生研究院介绍,这款疫苗的二期临牀试验已于五月底招募志愿者。莫德纳公司将于七月二十七日启动三期随机双盲对照临牀试验,旨在进一步评估疫苗的功效、安全性和免疫原性。三期临牀试验将在全美八十七个地区进行,招募三万名志愿者。研究应会持续进行至十月二十七日,但初步结果应该早就会出炉。
据报,医学期刊《刺针》也将发布新冠疫苗的好消息。该疫苗由牛津大学团队研发,阿斯利康制药公司制造。《刺针》可能在今日公布疫苗早期临牀测试的结果。阿斯利康曾表示,最早可能在九月开始提供疫苗。辉瑞和德国生技公司BioNTech之前也宣布,两家公司共同研发的两款新冠疫苗已经获得美国“快速审”(Fast Track)资格。
根据世卫资料,目前全球约有一百六十种新冠病毒疫苗正在开发中。俄罗斯国防部昨日表示,在对一群志愿者进行临牀试验后,俄国已经研发出一种“安全”的新新冠疫苗。声明说,十八人接受试验,现已出院,没有“严重不良反应、健康抱怨、并发症或副作用”。
新冠疫苗研发入佳境 美国或夏季结束前大量生产
美国制药公司辉瑞(Pfizer)及德国生物科技公司BioNTech周一(13日)表示,双方合作研发中的两款新冠状病毒疫苗已获得美国食品及药物管理局(FDA)的“优先审理”(priority review)资格,意味FDA有机会在未来6个月内决定是否批准上述两款疫苗投入使用。该两款疫苗一旦获得FDA批准,最快会在本月底于3万名疫苗计划参与者的身上进行测试;若测试成功,两间公司预期今年底可生产多达一亿剂量的疫苗,明年底产量达到12亿剂量。
另外,有不愿意透露姓名的美国官员表示,与政府合作的药厂可以在四至六星期后开始制造疫苗,并于夏季结束前量产,目前政府正与制造商合作,准备疫苗生产设施及搜购疫苗原材料。
特朗普政府目标于2021年前生产三亿剂疫苗。该名官员指,政府与药厂合作研发的新冠病毒治疗药物临床试验结果将在未来数周出炉,预料到秋季时,有关药物将大量生产。
德国新冠疫苗突破 有望年底前上市
德国生物科技先驱BioNTech表示,新冠肺炎疫苗临床试验进展顺利,有望在年底获准上市,马上进行大规模接种。
总部位于梅因斯(Mainz)的BioNTech是德国生物科技的先驱,专精信使核糖核酸(mRNA)技术,去年10月在美国纳斯达克挂牌上市。
BioNTech原本主力是癌症治疗,最近改投入新冠肺炎疫苗的研发,结盟对象包括美国辉瑞药厂(Pfizer)和中国的复星医药,4月底获政府批准成为德国最早进行临床试验的新冠肺炎疫苗。
BioNTech创办人兼执行长沙辛(Ugur Sahin)接受《华尔街日报》访问时表示,临床试验的结果比原先预期还好,预计7月底进入第3期,届时将有3万人参与,有望在12月批准上市。
沙辛透露,只要疫苗一上市,即可在美国、欧洲和其他国家进行大规模接种。BioNTech与辉瑞合作,计划在年底前生产上亿剂,明年底前产量增加到10亿剂。新型冠状病毒疫情肆虐全球,各国科学家快马加鞭投入疫苗研发,包括BioNTech在内,目前已有十几种的疫苗进入临床试验。不过,沙辛表示,等到全人类的90%透过感染或接种对病毒免疫,才算真正战胜病毒,他估计还需要10年的时间。
民调:超7成加拿大人愿意接种新冠疫苗
【星岛综合报道】最新一项民调显示,在有新冠疫苗的情况下,有四分之三的加拿大人表示愿意接种疫苗。
Research Co.调查发现,超过7成的受访者对三级政府应对疫情的方式感到满意,而有近一半的人现在愿意在公共场合佩戴口罩。在5月份的最新民调以来,各省的满意度提高了11个百分点。就卑诗省而言,83%的省民对省府的应对表现感到满意,上升了14个百分点。
安省、魁省和亚省的大多数居民也对各自省府感到满意。此外,加拿大人出门时戴口罩的比例从5月的14%上升到6月的48%。
Research Co.总裁坎塞科(Mario Canseco)说:“外出佩戴口罩方面,男女之间存在很大的差异。在加拿大,57%的女性出门时会戴上口罩,而只有39%的男性会这样做。”
与此同时,多逹40%的加国国民正在清理他们的食品杂货以防止感染,而有23%的人由于担心感染而不再从餐馆订餐。有近30%的人承认在家里吃得比平时多,而近20%的人称,在家里饮酒更多了。另外有16%的人说他们更容易发脾气。
全国37%的人希望能够在今年12月前参加或举办大型社交聚会;还有26%的人希望能前往现场观看体育赛事。想出国旅游的人达到21%。有半数的加拿大人认为,新冠疫情最严重的时期已经过去。
V33
加拿大新冠疫苗最新进展:与葛兰素开始合作 与中国合作产生问题
全球积极进行新冠状病毒疫苗研发工作,加拿大与世界的几个生物和制药公司也有合作项目,最新消息是加拿大的Medicago公司与葛兰素史克药厂合作;此外,加拿大国家研究委员会(National Research Council of Canada)5月宣布与中国康希诺生物公司合作研发的新冠疫苗将进入人体测试阶段,但目前为止加国却尚未收到来自中国的疫苗试验剂。
全球最大的疫苗生产商葛兰素史克(GSK)着重的研究室将其疫苗加强剂技术应用于可能的新冠状病毒疫苗中,该疫苗佐剂会交由全球七家公司进行开发,其中包括加拿大生物制药公司Medicago。Medicago总部位于加拿大魁北克市,是私有企业。
Medicago在等待渥太华能批准将此技术用于流感疫苗中,它是以植物的叶子作为生物反应器来生产新型冠状病毒S-spike的三个刺突蛋白之一,然后可以与GSK的加强剂一起用于疫苗中。这个概念是在某些已存的疫苗中添加了佐剂或功效增强剂,以增强免疫反应,从而获得更持久的免疫力来预防病毒感染。
GSK周二表示,两家公司的目标是在明年上半年提供疫苗,并在2021年底前生产约1亿剂疫苗。三种不同剂量水平的早期人体试验有望在7月中旬开始 。
另一方面,加拿大国家研究委员会5月初宣布正和中国康希诺生物公司(CanSino Biologics)合作的疫苗开发,很快将进入人体试验。如今此疫苗在中国第一和第二期的临床实验已展开,并完成二期临床解盲,日前获得中国军方的批准供军队内部使用,有效期一年。但加拿大研究人员至今却仍未获得疫苗。
负责疫苗计划的达尔豪西大学加拿大疫苗学中心和联邦卫生部都无法回应是甚么原因导致中国疫苗运送延迟的原因。
达尔豪西大学加拿大疫苗学中心(CCfV) 主任哈普林(Scott Halperin)周一在国会卫生委员会说,仍在等待道德批准,希望能很快进行试验。
根据与CanSino达成的协议,如果证明有效,加拿大将能够在国内生产疫苗并将其提供给加拿大人民。加拿大不能享有任何知识产权或被允许贩售疫苗。
目前全球尚无正式批准的新冠状病毒疫苗,但已有19种疫苗在进行人体试验。
网上图片
v01
加国生物公司参与研发 新冠疫苗临床数据喜人
温哥华一家生物科技公司,正积极参与一项有关新冠疫苗的研发中。目前该疫苗已经进行临床试验,最快有望在明年正式面市。
坐落在卑诗大学(UBC)校园内的温哥华生物科技公司Acuitas Therapeutics,从2009年以来就专门致力于开发以脂质纳米颗粒(LNP)为基础的核算治疗先进递送系统(delivery system)。这项技术也被运用到合作伙伴、德国BioNTech公司的新冠疫苗研发当中。
BioNTech公司与全球最大制药公司辉瑞(Pfizer Inc.)日前宣布,双方共同研究的新冠疫苗已取得初步临床数据,获得令人鼓舞的人体试验结果。该疫苗融入先进mRNA技术,可令人体产生触发免疫反应的蛋白质,而非常规疫苗利用“杀死或减弱病毒”来产生免疫反应有所不同。
注入体内mRNA保护可达细胞
Acuitas Therapeutics公司总裁兼首席执行官马登(Thomas Madden)表示,如果将mRNA直接注入体内,会迅速分解无法抵达细胞,而公司研发的递送系统可以为mRNA提供保护,并将其运送到细胞内。他解释:“想像一下你从网上购买了一个非常易碎的玻璃饰品,通过Acruitas递送技术,该饰品都会被仔细封装,无论旅途多么艰辛,都会受到很好保护并都顺利送达家中。它还会自行打开前门入内,将包装拆开后把装饰品留在你的门前走廊。”
马登补充,mRNA疫苗最大的优势之一是它的开发速度比传统疫苗要快得多。他说:“我们可以潜在地更快展现疫苗的安全性和有效性,并使它们更快投入使用。在扩大生产方面有时也比常规疫苗更加简单直接。”
目前BioNTech与辉瑞对mRNA疫苗的研究工作仍在继续。马登透露,预计最快要到2021年才能就绪。
Acuitas Therapeutics的相同技术,同时也被欧洲其他合作公司使用,以期尽快消灭全球性新冠疫情。
加研发新冠疫苗伙伴 具中国军方背景惹议
■■渥京伙拍的康希诺生物公司。网上图片
星岛日报讯
加拿大正与中国一间药业公司合作研发新冠疫苗,并将进入人体测试阶段,但该药业公司有中国军方背景,加拿大在该项研究上的投资受到质疑。
据《国家邮报》(National Post)报道,当总理杜鲁多上个月宣布加拿大即将对一种新的新冠病毒疫苗进行人体试验时,引起了很多兴奋和困惑。该疫苗的开发者是一家名为康希诺生物(CanSino Biologics)的中国公司,在制药行业鲜为人知。
康希诺生物不仅与中国军方医学科学部门合作,是国际上寻找新冠疫苗的领先者,而且与加拿大有着深厚的渊源。
曾一起研发伊波拉疫苗
加拿大方面负责新冠疫苗研发的国家研究委员会(National Research Council of Canada),此前已与康希诺生物公司合作研发伊波拉(Ebola)疫苗,并且国家研究委员会以及麦克马斯特大学(McMaster University)的科学家,还与康希诺生物公司一起合作研发了结核疫苗。
加拿大国家研究委员会上个月宣布,与康希诺合作开发被称为“Ad5-nCoV”的疫苗,这个疫苗今年早些时候获得了中国监管部门批准,使得康希诺生物股份公司得以在中国进行人体临床试验。目前加拿大疫苗学中心共有45人组成一个团队研究“Ad5-nCoV”。
但是,在加拿大和中国之间的关系恶化之际,一些专家对渥太华对该项目进行投资的决定提出了质疑。
第一阶段测试 疫苗并不可靠
渥太华大学健康政策教授阿特兰(Amir Attaran)认为,这些早期试验结果显示其功效仍是未知数,而其他COVID疫苗似乎更有希望,并得到西方主要大学和公司的认可。他质疑加拿大为何不选择投资其他的疫苗研发,却选择有中国军方背景和中国公司作为首选合作伙伴。
魁省拉瓦尔大学(Laval University)微生物学和传染病学系教授、该校传染病研究中心主任科宾格(Gary Kobinger)说,他实际上对加国政府抛开政治歧见而与中国合作表示称赞。 但是他认为,第一阶段的测试结果表明,康希诺生物公司的疫苗并不可靠。
他说:“这个疫苗平台将面临很多挑战……到最后有点像赢得彩票。这就是为什么我对此有些困惑。 我还是不明白,那是如何运作的? 投资于此的决策机制是什么?”
总理杜鲁多于5月12日宣布,加拿大已与这家总部位于天津的康希诺生物公司达成协议,进行第一阶段另一轮试验,以从根本上衡量该疫苗是否安全并产生免疫反应,如果成功,则进入第二阶段和第三阶段试验。
联邦政府拒绝透露投入该项研究的费用,表示与康希诺生物公司合作协议的细节受到“商业机密”保护。 不过,渥太华已经宣布,将投入10亿元用于COVID-19研究。
联邦买3700万支注射器 新冠疫苗到时一人一针
(■联邦已着手洽购未来疫苗注射将使用的注射器。美联社)
疫苗研发的脚步不断进展中,渥太华为了预防物资短缺的问题,已经先与厂商签订了3,700万支的注射器合同,让未来疫苗注射的过程更顺畅。
总理杜鲁多宣布,注射器已添加到因应新冠状病毒的采购必要耗材清单中。联邦采购部长阿南德(Anita Anand)表示,已与加拿大公司Becton Dickinson Canada签订合同,以供应提供疫苗的工具。阿南德没有提供注射器交货的时间表,指出目前的需求并不那么紧迫。
联邦首席公共卫生官谭咏诗说:“我们需要提前计划,也会安排如何将疫苗优先用于某些人群中。”
已备妥上亿个外科口罩
5月中旬,加拿大卫生部宣布已批准该国可能的疫苗临床试验,加拿大并参与世界各地正在进行的试验。传染病专家沙卡维(Abdu Sharkawy)说:“虽然没有紧迫的需求,但这场疫情让我们体认到未雨绸缪的重要性,及早反应准备肯定没有伤害。”
杜鲁多指出,加拿大已收到超过1亿个外科口罩,而这只是政府订购的三分之一。他还指出,已经采购了近4,000万个手套。
随着更多的企业和部门重新营业,对个人防护装备(PPE)的需求只会增加,杜鲁多说,过去两个月中,联邦政府不断与加拿大厂商合作来生产医疗物资,这不仅对公共卫生安全至关重要,也创造了许多加拿大人的工作机会。
悲报!牛津疫苗研发失败 未能阻止猴子感染新冠
据外媒报道,牛津大学的COVID-19疫苗在试验中未能阻止猴子被新型冠状病毒感染,这打破了英国今年对拥有安全有效疫苗的希望。该疫苗是目前正在人类身上测试的顶级候选药物之一。但是动物试验的详细结果表明,ChAdOx1 nCoV-19疫苗不能阻止猕猴感染病毒,也不能阻止动物将感染传播给其他人。
之前有报道说美国投了12亿美元,试图优先获得3亿剂疫苗,看来这些是打水票了。点击可以查看之前本站关于疫苗战争的报导:特写:全世界疫苗战争 美国到处撤钱要抢头汤
(都市网Rick综合)
安省政府拨720万研发疫苗 下周将推新检测计划
安省省长福特表示,已为15个疫苗研发项目提供720万元资助,另外,预期下周会推出提高病毒检测数量的计划,希望有更多人可接受病毒检测。
福特表示,省府于上月拨出2,000万元用作疫苗研发基金,目前正为15个“最有希望”的项目提供总值720万元资助;福特强调,在未找到合适疫苗前,仍要与新冠病毒作斗争。
安省专上教育厅长罗马诺(Ross Romano)表示,省府所选择的研发项目,是具有“合理成功机会”。
另外,福特表示,正敦促公共卫生部门提高病毒检测能力;他表示,希望见到货车与的士司机、汽车业与食品处理厂雇员,以及没有病征的省民,能够接受病毒检测。他表示,最近5天已看到新增感染数字上升,但检测数字没有同步增加,情况令人感到忧虑。
福特称,省府下周会推出一项提高病毒检测数量的计划;他表示,会专注进行随机检测。
他表示,省府愿意考虑容许餐饮业扩大露天经营面积,下次举行的省议会会议上,将会讨论有关建议。星岛综合报道
美研究指猴子染疫后产生抗体 疫苗有望成功
正当各国科学家致力研发疫苗之际,两项以猴子为对象的研究报告,为人类寻找方法对抗新冠肺炎病毒带来希望。其中一项研究发现,恒河猴感染了该种病毒及出现病症后,体内产生有保护作用的抗体,数天后康复。另一项研究,则利用仍在试验中的候选疫苗注射入恒河猴体内,令牠们产生有保护作用的抗体。
这两项研究报告都在《科学》杂志内发表。其中一份报告的作者、美国波士顿病毒及疫苗研究院院长巴鲁奇表示,这两项研究工作十分重要,因为人类感染了新冠肺炎后能否自动产生抗体及免疫力,科学家仍然所知不多。
第一项研究由巴鲁奇和他率领的团队进行,对象为9只成年恒河猴,故意让牠们感染新冠肺炎病毒。牠们都出现病症。专家发现猴子体内出现有保护作用的抗体,数天后陆续痊愈。
为了证明牠们已经拥有免疫力,科学家在35天后再次让牠们接触该种病毒,进行所谓“再挑战”的测试,那些恒河猴再没有出现病症,显示牠们不再受到感染。
不过,研究团队警告称,他们需要进行更进一步的研究,了解猴子感染病毒和人类感染病毒的异同,才可作出结论。
第二项研究由亚裔病理学家 Jingyou Yu 和他的团队进行,替35只成年恒河猴注射仍在试验中的候选疫苗,观察牠们的反应。6周后,牠们再度获安排接触新冠肺炎病毒,结果发现牠们血液中的抗体数量,足以对抗病毒。
同样,科学家强调需要进行更进一步的研究,才可确定疫苗发挥保护功效可以维持多久,以及了解替人类注射疫苗的理想份量。
画饼充饥?英国拟九月供应3000万剂疫苗
英国政府周日宣布增加拨款加速研发疫苗,其中牛津大学的研发项目进展良好,该校已和阿斯利康药厂达成协议,一旦疫苗证明可行,将在九月底前向英国提供三千万剂疫苗。
英国国际发展大臣岑浩文周日在唐宁街见记者,表示新冠药物和疫苗研究工作“进展良好”、“速度空前”。牛津透过数家实验室,招募了一千一百零二名首批临牀试验参与者,随机接种疫苗或安慰剂,他们在本周较早前已接种。试针者年龄介乎十八至五十五岁,必须是未受过新冠病毒感染的人,健康良好,无怀孕或喂哺乳。帝国理工学院也会在六月展开测试,十月再进行另一轮测试。
英国当局将为进展较快的两个疫苗研发项目,额外增拨八千四百万英镑(约七亿九千万港元)加速研发,其中六千五百五十万英镑资助牛津大学,帝国理工学院则可获一千八百五十万英镑。牛津大学在政府支持下,已经和英国阿斯利康药厂敲定一份全球许可协议,用于疫苗的商业化和生产。疫苗还须通过安全和效能检测才能量产应用,但阿斯利康表示,若疫苗真的有效,会在疫情下不惜代价生产出来。
岑浩文说:“如果疫苗研发成功,阿斯利康九月会提供三千万剂予英国,即协定生产一亿剂的一部分,英国将会是首个获取疫苗的国家。政府也会确保除了英国民众外,能够以最低成本,将疫苗供给发展中国家。”
根据世界卫生组织(WHO)上周六公布的名单,目前全球有一百一十八个新冠疫苗研发计画正在进行,其中欧美和中国的八种疫苗已进入临牀试验阶段,以确认对人体的安全性和有效性。美国已有两种新冠疫苗开展一期临牀试验,分别是mRNA-1273信使核糖核酸(mRNA)疫苗和INO-4800脱氧核糖核酸(DNA)疫苗。前者由美国生物科技公司Moderna与国家过敏症和传染病研究所在三月展开临牀试验,对四十五名健康者用药两次,被指定为食品及药物管理局(FDA)的优先审查对象;后者由美国药厂伊诺维奥(Inovio)开发,在四月开始了试验。
中国已启动四种疫苗试验,包括利用无病原性病毒的灭活疫苗。在欧洲,德国生物科技公司BioNTech正在和美国制药巨头辉瑞进行联合试验。日本也有六种疫苗进入名单,当中有些已进入动物实验阶段,但均未开始临牀试验。东京大学医科学研究所教授河冈义裕认为:“即使外国的疫苗获得特例批准,国内的供给量也会很有限。在年内普及很困难。”
美国总统特朗普上周五表示,期待今年底前研发出新冠疫苗。特朗普称,美国政府专家一直在评估全球约一百种新冠候选疫苗,认为其中十四种很有希望,并正努力进一步缩小这份名单。此外,制药企业通常要等到疫苗获批后才开始生产,但这会延误向公众提供疫苗的时间。鉴于目前任务紧逼,在“曲速行动”计画下,美国政府将在疫苗获批前就投资生产最有希望的候选疫苗。
新冠疫苗试验结果喜人 美股欢欣鼓舞
(■5月18日,在美国首都华盛顿,一名戴着口罩的男子准备骑自行车健身。新华社)
美股道琼斯指数18日飙涨911点,与标普五百指数涨幅皆逾3%,创一个多月来最佳表现。新冠肺炎疫苗临床试验报佳音,振奋市场人心,助大盘走出上周创近两个月最糟表现的阴影。
美国生技厂商莫德纳(Moderna)公布,新冠病毒疫苗首阶段临床试验取得正面结果。部分健康志愿者施打疫苗后体内产生免疫反应。
根据一项小规模首次人体试验的数据样本,来自莫德纳的实验性疫苗显示出有希望的早期迹象。莫德纳18日在公告中表示,这项研究的主要目的是观察疫苗的安全性,在小型第一阶段试验中未显示重大警告信号。该试验与美国政府联合进行,莫德纳计划继续推进更广泛的试验。第三阶段试验将在7月展开,届时会有大量志愿者参与。
研究人员检查了试验对象的血液样本,以及疫苗是否帮助他们产生了可以抵抗病毒的抗体。研究人员发现,在这项研究中使用的两个较低剂量水准下,在第二次巩固注射后发现的抗体水准等于或超过感染康复患者的抗体水准。
“这是一个非常好的信号,表明我们产生了可以阻止病毒复制的抗体,”Moderna首席执行官Bancel接受采访时表示。他说,数据“好得不能再好了”。Bancel说,安全性似乎良好,反应是典型的疫苗反应。他说,这些反应症状包括注射部位疼痛和发红,以及迅速自行消失的暂时性发烧或发冷。
疫苗初步试验结果激起旺盛买盘,道指终场飙涨911.95点,涨幅3.85%,收在24597.37点。标普五百指数大涨90.21点,涨幅3.15%,收在2953.91点。以科技股为主的纳斯达克综合指数劲扬220.27点,涨幅2.44%,收在9234.83点。
道琼斯指数与标普五百指数都创4月上旬以来最佳单日表现。道琼斯指数30档成分股共29档收红;标普五百指数11大类股全面走扬,在国际油价大涨8%带动下,能源股飙涨7.6%,表现一马当先。
受疫苗试验结果激励,莫德纳股价飙涨20%,攻上历史新高80美元。
100%产生抗体! 全球首个新冠人体试验结果曝光
疫情席卷全球以来,全世界的科学家、医疗科技公司都在为疫苗研制快马加鞭地努力。
今天有一个好消息,全球首个疫苗人体试验结果公布,全部受试者体内发现抗体,另外至少8人体内发现病毒中和抗体!
消息一出,全球为止振奋,研发这个疫苗的公司股票更是狂飙240%。
100%受试者发现抗体
Moderna公司周一表示,这款疫苗名为mRNA-1273,第一期人体试验有了积极的结果。
该研究的所有45名参与者都接受了三种不同剂量的疫苗,Moderna说,它看到了疫苗在参与者体内激发免疫反应的能力。
参与试验的有45人,平均分为3组,接受不同剂量的疫苗,每人接种两次,中间间隔28天。剂量分别为25微克,100微克和250微克。
全部45名受试者体内都出现了结合抗体,其中25微克和100微克组的前4人共8人体内发现病毒中和抗体,类似于在康复患者中发现的抗体。250微克的具体数据还未公布。
中和抗体与病毒结合,使其无法攻击人类细胞。
美国国家研究院(National Institutes of Health)进行的这项研究的早期结果显示,八名注射Moderna疫苗参与者的抗体水平与COVID-19痊愈者的血液样本中抗体水平相似。
Moderna首席医学官塔尔·扎克斯(Tal Zaks)博士说:“我们已经证明这些抗体,这种免疫反应,实际上可以阻断病毒。” “我认为这是我们获得疫苗的旅程中非常重要的第一步。”
一位不参与Moderna工作的疫苗专家表示,该公司的结果“很棒”。
美国研究院专家保罗·奥菲特(Paul Offit)博士说:“这表明该抗体不仅与病毒结合,而且还阻止了病毒感染细胞。”
该公司的疫苗在研发快速传播病毒的治疗方法中处于最前沿,上周获得了美国卫生署的“快速通道”标签,从而加快了监管审查的速度。Moderna预计将从7月开始进行规模更大的后期试验。
耐药性和副作用研究
药物开发人员说,在早期研究中,人们还发现这种疫苗,mRNA-1273是安全的,并且耐受性良好。
该试验中有一个人在注射部位周围发红,这被称为“ 3级”副作用。
另有三名参与者以250微克的剂量接种疫苗时出现了发烧和其他类似流感的症状。
接下来将进行大规模临床试验
这些早期数据来自一期临床试验,该试验通常研究少数人群,重点研究疫苗是否安全并引发免疫反应。
美国食品药品监督管理局(FDA)已批准该公司开始进行通常涉及数百人的二期试验,而Moderna计划于7月开始进行称为3期试验的大规模临床试验,该试验通常涉及数万人。
Moderna预计剂量的第3期研究将在25到100微克之间。
到目前为止,Moderna研究的受试者接种了25和100微克的疫苗,其抗体水平也与自然感染冠状病毒的人相似或更高。
Zaks博士对CNN表示,如果未来的研究进展顺利,该公司的疫苗最早将于1月份向公众提供。
扎克斯说:“这绝对是好消息,我们认为许多人已经等待了很长一段时间。”
由美国国家研究院(National Institutes Health)领导的这一研究结果尚未经过同行评审或发表在医学期刊上。
疫苗最早明年1月上市
今年1月,美国国家过敏和传染病研究所所长Anthony Fauci博士表示,疫苗上市大约需要12到18个月。他预计该疫苗最早将于明年1月上市。
Moderna公司已与瑞士合同制药商Lonza Group AG和美国政府签署了生产大量疫苗的协议。
根据世界卫生组织的资料,总部位于马萨诸塞州剑桥的Moderna是全球八家研究新型冠状病毒疫苗并进行人类临床试验的开发商之一。辉瑞公司(Pfizer)和Inovio也在美国,另外一家在英国牛津大学,其余四家在中国。
根据美国霍普金斯大学发布的统计数据显示,截至5月18日11时左右,全球新型冠状病毒肺炎累计确诊病例已超过470万例。如果疫苗制生成,确实是关乎全人类福祉的事情。
希望生活能早日恢复正常。
参考资料:https://www.ctvnews.ca/health/coronavirus/early-results-from-moderna-vaccine-trial-show-participants-developed-antibodies-against-coronavirus-1.4943881
https://www.cnbc.com/2020/05/18/moderna-reports-positive-data-on-early-stage-coronavirus-vaccine-trial.html
https://globalnews.ca/news/6955735/coronavirus-vaccine-moderna-trial/
编辑:小星 言西早