Tag: 新冠疫苗
加拿大疫苗研发首期成功 100%产生抗体反应
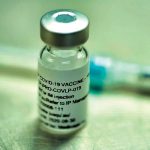
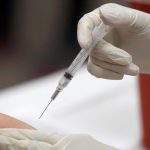
在美国辉瑞大药厂(Pfizer)和德国BioNTech联手研发的新冠疫苗取得成功之际,魁省公司Medicago也传出佳音。Medicago周二宣布,该公司研发的疫苗第一期临床试验的中期结果发现,在接受两次候选新冠疫苗接种后,100%受试者产生了抗体反应。
100%试用者产生抗体反应
联邦政府已与Medicago签署协议,以确保购买7,600万剂该公司的疫苗。此外, Medicago还将从渥太华获得1.73亿元的资金,用于研发疫苗和在魁北克城建设厂房。
周二全国有8个省份报告共新增4,303确诊,累计273,037宗。新增死亡68人,累计10,632人。全国目前有41,008个现存病例,221,279名患者已康复。
新增病例方面,魁省新增1,162宗,总数117,151宗;安省增加1,388宗至86,783宗;亚省增713宗至34,873宗;卑诗省增525宗至19,239宗;缅省增384宗至8,878宗;沙省增127宗至4,214宗;新斯高沙省增3宗至1,132宗;爱德华王子岛增1宗至67宗。
在死亡数据方面,魁省新增38人至6,493人死亡;安省增15人至3,260人;亚省增7人至376人;卑诗省增3人至284人;缅省增5人至114人。全国其余8个省区当天无报告新增死亡案例。星岛综合报道
杜鲁多为辉瑞疫苗叫好 加拿大早已预定2000万剂
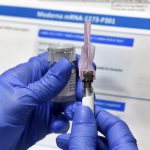
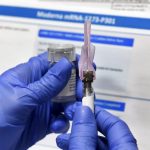
【加拿大都市网】美国药厂辉瑞(Pfizer)和德国BioNTech研发的新冠病毒疫苗试验数据,显示这款疫苗的有效抵御新冠病毒的有效率高达90%。听到疫苗的好消息,总理杜鲁多(Justin Trudeau)也感到振奋。
杜鲁多周一早上对记者说,加拿大可以看到“隧道尽头的曙光”了,但我们还没有走出困境。
杜鲁多重申政府预计最有希望的时间表,预估明年初疫苗能在加拿大上市。
他仍然敦促加拿大民众继续保持社交距离,并遵守公共卫生准则,共同来抑制疫情扩散。杜鲁多说:“非常清楚的道理,如果你在接下来的几天和几星期内感染新冠病毒,疫苗不会对你或你的家人有所帮助。”
他说:“我们看到隧道尽头的光。我们希望能够到达那里,但是我们需要尽自己的一份力。我们要保持坚强,至少还有几个月时间。”
加拿大已经与辉瑞公司达成了一项协议,当疫苗问世时,加拿大将购买2,000万剂疫苗。
辉瑞和合作伙伴BioNTech希望今年年底前生产5,000万剂新冠疫苗,并在2021年提升疫苗产量至13亿剂。辉瑞公司临床开发高级副总裁格鲁伯(Bill Gruber)说:“这是令我们感到鼓舞的好消息。”
图:星报
v01
联邦为明年新冠疫苗做准备 寻分销及存储商
【加拿大都市网】联邦政府现正就未来3到5个月内可能推出的新冠疫苗做前期准备,其中包括寻找合适疫苗分销及存储商等。
政府合同网站上刊登一则通知,邀请有兴趣竞标的公司进行资格预审。有关官员表示,他们计划在这个月底之前完成这项工作。
根据通知的内容,政府正在寻找一间或多家公司,“在必要的情况下,为执行新冠疫苗后勤战略,提供广泛的物流及支持服务。”
通知接着指出,其中大部分工作将涉及疫苗的安全管理和迅速分发,包括向偏远的郊区派送。
希望承接这项工作的供应商必须证明,如果出现需要大规模推广和分发的紧急状况,他们有能力在48小时内部署到全国各地。
通知还称:“预计疫苗将在在2021年第一季度开始分阶段投入使用,一直持续到2022年。经联邦政府确认,2021年第一季度是指1月至3月。符合资格的公司必须能够在2020年12月15日前开始工作,为这些计划做准备。
通知又指,安全性将是至关重要的,鉴于疫苗的巨大价值,它们可能会成为犯罪分子的目标,因此必须在任何时候都保护好疫苗。
加拿大首席公共卫生官谭咏诗(Theresa Tam)博士在周五的记者会上说,她对2021年第一季度的疫苗供应持“谨慎乐观”态度。
总理杜鲁多(Justin Trudeau)表示,有望在今年春天推出疫苗。
V33
联邦拨2.14亿元支持本国新冠疫苗研究
【加拿大都市网】联邦政府表示将拨款2.14亿元,支持“加拿大制造”的新冠病毒疫苗研究。
总理杜鲁多周五公布,新拨款共2.14亿元,其中1.73亿元将提供魁省为本部的Medicage公司,而温哥华的Precision Nano Systems则获1820
万元作研发和测试。与Medicage的合约包括最多达7千6百万剂候选疫苗,以及在魁北克巿设立一生产设施。另还有2千3百万元拨供加拿大全国研究议会。
杜鲁多在渥京的记者会表示:“这是支援研究工作的同时,稳定提供给国民的潜在疫苗。”联邦政府至今已花费超过10亿元,以保证新冠病毒新疫苗提供的剂量,并已与6间药厂巨头达成协议,加拿大亦通过COVAX成为国际疫苗联盟的一部分。
杜鲁多称:“加拿大已有潜在疫苗的优秀投资组合,但我们亦知道,暂仍无人得到那成功疫苗。”他表示,合理的预期是该疫苗可能在明年某些时间推出,但将是小量供应,且首先只提供给优先群组如前线工作人员和最易受感染的脆弱人口注射疫苗。
加拿大周四公布新冠个案的纪录性增长数字,有近2800人新确诊。杜鲁多强调:“我们需要将这些个案数目回降,这是严重而人人必须尽上本分的。”
(图:Global News) T05
为加快疫苗研发 英国准备让年轻人「以身试毒」
(■世界卫生组织20日发布的最新数据显示,全球累计新冠确诊病例已超4000万例。目前全球都在渴望疫苗解救新冠疫情。美联社)
英国政府计划推动一项抗疫实验,拟刻意令健康的年轻志愿者感染新冠病毒,以研究足以令人染疫的最少病毒量,希望有助加快新冠疫苗的开发。据悉,试验最快将于明年1月展开,首阶段将有90名志愿者参与。
英国政府20日公布该项挑战计划,这将是全球率先以此方式进行人体试验的国家。据中央社报道,英国商业、能源及产业策略部(BEIS)发布新闻稿指出,政府将斥资3360万英镑与伦敦帝国学院、实验室hVIVO,以及皇家自由医院伦敦国家医疗保健服务基金会信托等单位合作加速研发疫苗。
在上述计划中,健康的成年受试者自愿被施打初步已获证明安全的候选疫苗,接着在安全且受控制的环境下,暴露于病毒当中。医护人员与科学家将24小时严密监控,观察受试者对疫苗的反应及有无副作用。新闻稿指出,研究人员将使用控制的病毒剂量,试图找出让一群年纪在18至30岁的健康年轻人感染的最少病毒量为多少。这项计划将征求最多90名受试者,投入实验的时间将获得报酬。
18至30岁是目前被认为感染新冠病毒疾病后风险最小的族群,加上受试者条件必须健康良好,预料能把风险降至最低。由于蓄意让人感染目前尚无药可治的新冠病毒具有道德疑虑,BEIS表示,任何临床实验在开始进行前,都必须受到英国药品及保健品管理局及NHS健康研究管理局严密审查。
人体实验在过去数十年加速疫苗研发,包括疟疾、伤寒、诺如病毒与流感疫苗等。这项研究计划通过审查后,预料最快将于明年1月展开,在最严格的条件下进行,包括出入管制、废弃物控管等。研究结果预料于明年5月出炉。BBC报道指出,全球目前共有数百组疫苗研发正在进行,速度最快的例如牛津大学已进入最后测试阶段。虽然新冠疫苗可能在“人类挑战”计划开始前就宣告完成,甚至投入使用,但科学家认为这项计划依旧有价值,将可比较究竟哪项疫苗更加有效。
疫苗上市后面临数量不足
目前疫情加速蔓延,全球都渴望疫苗解救疫情,但年轻与健康族群可能要多等一年才有机会接种。据《华盛顿邮报》报道,世卫专家史瓦米那尚早前在一场世卫的线上QA会议里说:“人们心里的如意算盘是‘等明年1月1日或4月1日我就能打到疫苗,然后就能重拾往日正常生活’。可惜到时不会是这样的,届时会有一堆指南出炉,我觉得一般人,以及健康的年轻者,可能要等到2022年才接种得到疫苗。”
联合国儿童基金会首席免疫专家南迪说:“疫苗开始能上市的头几年里,数量不足以供今日全球70亿人施打,只能零零星星地慢慢等。”他说,包含医卫与教育等基础服务人员应先施打,因为人们仍需活在疫情下好一阵子,需要相关体系持续运作。
辉瑞称下月申请紧急使用授权 有望成美国首面世新冠疫苗
美国药厂辉瑞公司(Pfizer Inc.)表示,预计将会在11月下旬在美国申请其正在研发的新冠疫苗的紧急使用授权。如果申请成功,意味着该疫苗可能在今年年底在美国面世。
辉瑞称,有望于本月获得数据,以确认这种疫苗是否有效。同时,辉瑞还需要约4.4万人规模的临床试验的安全性数据,安全性数据预计将于下个月获得。
目前辉瑞公司正在研发的新冠疫苗是与德国生物技术公司BioNTech共同合作开发的核酸RNA疫苗,但这种疫苗尚无商业化先例,技术和生产工艺以及物流方面仍有待进一步验证。
这是美国制药厂商首次明确疫苗上市申请时间表。辉瑞CEO布尔拉(Albert Bourla)上周五表示:“假设数据是积极的,辉瑞将在11月第三周实现安全里程碑后,在美国申请紧急授权使用。”BioNTech的发言人也确认了该时间表。
目前全球都在指望疫苗的问世,以帮助控制新冠病毒的传播。新冠病毒已经造成全球超过100万人死亡,美国感染人数也突破了800万,新冠疫情还严重破坏了全球经济。
世卫组织总干事谭德赛上周表示,人们有望在今年年底接种新冠疫苗。目前全球已经有10种实验性的疫苗进入临床三期阶段。
中国新冠疫苗将在北京武汉开放接种 出国留学生优先
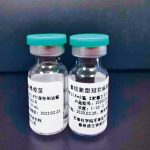
据《科创板日报》记者从知情人士处获悉,目前中国国药集团新冠疫苗已经在北京和武汉开放预约接种。具体可以通过国药集团官网或扫描国药集团提供的二维码进行预约,预约者在约2周后收到通知,并到指定地点注射。
据了解,虽然所有人群都可以进行预约,但是公司会优先选择出国留学生,特别是今年11月至明年1月需出国的留学生进行接种。记者查询国药集团官网后暂未发现报名通道,公司官网电话亦忙音中,不过通过一款“新冠疫苗接种预约”的小程序可以看到,目前已有逾7万人进行了接种报名。(《科创板日报》记者 徐红)
加拿大卫生部将审批牛津新冠疫苗
【加拿大都市网】加拿大卫生部周五,他们日前收到了阿斯利康公司(AstraZeneca)与牛津大学合作研发的新冠疫苗的首份批准申请。这是加国应对疫情流行的重要一步,但这也只是取得安全有效疫苗道路上第一步。
加拿大卫生部官员说,他们现在将对检测数据进行滚动筛查。9月,联邦政府政府批准了疫苗滚动筛查程序。该过程允许公司一旦拥有有效数据时就可提交,有助官员快速查看到重要信息并加快审批流程。
加拿大卫生部未有透露对阿斯利康公司与牛津大学合作的候选疫苗审查需要多久时间。但是在一份声明中,加拿大卫生部表示,当局暂不会做出决定,直到他们所已经收到支持该疫苗安全性、功效和质量的必要证据为止。
此外,联邦政府已经与阿斯利康公司达成协议,如果疫苗成功的话,加国将获得2,000万剂新冠疫苗。
加拿大卫生部表示,预计未来几个月,他们将收到疫苗测试的呈件申请。
上个月,一个志愿者在患上“潜在无法解释”的疾病后,阿斯利康公司的全球新冠疫苗试验被搁置。这是在该公司宣布疫苗已进入其临床试验的第三阶段后的几天暂停了。不过,据悉,相关的测试不久后又恢复了。
V33
即使新冠疫苗上市 4成加拿大人仍会先观察一下
【加拿大都市网】虽然很多人都表示向回到疫情之前的状态,但有调查显示,就算有新冠疫苗,约4成受访国民会先观察一段时间才注射。
在过去几个月中,说要立即接种疫苗的人数实际上有所下降。民意调查机构Angus Reid Institute最新研究发现,只有39%的受访者表示他们希望尽快获得疫苗注射,不到一半的人表示接种疫苗前要稍等一会儿。约16%的人坚决反对疫苗,只有7%的受访者表示不确定。
民调结果显示,自从夏季中期以来,表示一有疫苗就要立即接种的人数下降了7%。7月下旬首次对加拿大人进行这项调查时,有46%的人都说准备好了一有疫苗就立即接种。
在某些省府人们对疫苗的抗拒程度似乎更高一些。调查说:“值得注意的是,人均感染率最高的两个省份——亚省和魁省,他们不仅对疫苗接种的抗拒程度最强,而且自夏天以来就立场变得更为坚定。”研究称,大部分抗拒疫苗的原因可能是担心由疫苗引起的副作用。。
与此同时,越来越多的人在公共场合佩戴口罩。调查显示,84%的加拿大人表示,他们在公共场所“总是或大部分时间”佩戴口罩。自7月以来,这一数字增加了30%。
v16
新冠疫苗变鲨鱼浩劫 或致50万条被杀
为对抗新冠疫情,各国医学专家无不致力研制对症下药的疫苗,而疫苗中除了以现阶段的医药调配之外,美国加州近日出现用“角鲨烯”所合成的疫苗,未来可能将加入临床试验,消息一出立刻引起生态组织关注。事缘“角鲨烯”是从鲨鱼肝脏中提取的天然油,为获得生产疫苗所需要的“角鲨烯”,可能会导致多达50万条鲨鱼被宰杀。
“角鲨烯”拥有超高的医学价值,目前有几款流感疫苗中含有鲨烯,其作用可以提高免疫力,进而让疫苗的效力提高。英国制药大厂葛兰素史克(GlaxoSmithKline)目前在流感疫苗中便使用鲨鱼的“角鲨烯”。葛兰素史克今年5月曾表示,将生产10亿佐剂,可能用于生产对抗新冠肺炎的疫苗。而提取1吨“角鲨烯”则需要大约300条鲨鱼。总部位于美国加州的鲨鱼保育组织“鲨鱼同盟”(Shark Allies)指出,如果全世界每人接种一次含有“角鲨烯”的抗新冠肺炎疫苗,将需要宰杀约25万条鲨鱼,具体数量取决于“角鲨烯”的使用量。如果需要对全球人口进行两次免疫接种,则被宰杀的鲨鱼数量可能会增至50万条。据环保人士估计,目前每年大约有300万条鲨鱼被杀,用于提取“角鲨烯”。“角鲨烯”也用于化妆品和机油中。他们担心,对鲨鱼肝油的需求突然上升,可能会威胁到很多富含“角鲨烯”却已很脆弱的物种,如大西洋刺鲨。
据悉,为了避免威胁鲨鱼种群,目前已有科学家开始研发一种“角鲨烯”的替代品,这种替代品是由发酵甘蔗制成的合成物。“鲨鱼同盟”创办人兼执行总监布伦德尔(Stefanie Brendl)表示团体并没有试图减慢或阻碍疫苗的生产,只是要求在利用鲨鱼“角鲨烯”的同时,可以进行非动物源材料的测试,以便能尽快代替“角鲨烯”。团体表示从野生动物身上得到的某些东西永远不会可持续,尤其是不会大量繁殖的野生动物。
目前已经有网上联署书,呼吁大家加入停止使用鲨鱼体内的“角鲨烯”进行疫苗开发;此外令该组织忧心的是,宰杀鲨鱼的危机可能会出现在一些渔业监管不严密的国家。
加拿大再订2000万剂新冠疫苗
【星岛综合报道】总理杜鲁多宣布,加拿大再签署一项疫苗订购协议,获2,000万剂新冠疫苗;与此同时,加拿大将加入一个国际联盟,拨款4.4亿,参与全球疫苗分发。
杜鲁多周五在渥太华举行的记者会上宣布,与阿斯利康制药公司(AstraZeneca)达成一项协议,以获取正在牛津大学开发的疫苗,数量达2000万剂。
加拿大此前已与赛诺菲(Sanofi)、葛兰素史克(GlaxoSmithKline)、强生(Johnson&Johnson)、诺华(Novavax)、辉瑞(Pfizer)和莫德纳(Moderna Inc.)达成了疫苗协议,共计2.82亿剂。再加上周五宣布的阿斯利康制药公司,联邦政府已从不同制药公司订购六种领先疫苗。
杜鲁多说:“从一开始到现在,我们一直以科学为指导,COVID-19疫苗工作组和免疫工作团队都在开展重要工作,以帮助我们确定最有希望的疫苗选择和策略。”
尽管有疫苗已进入临床试验和开发阶段,但目前尚未有正式获淮用于COVID-19。 联邦公共服务与采购部长阿南德(Anita Anand)表示,全球市场激烈且不可预测,一旦疫苗研制成功,加拿大已经做好准备。
加拿大卫生部表示,将审查每种疫苗的安全性、功效和生产质量方面的证据,才决定是否会批准其在加拿大使用,只有获得批准之后才会提供给国民。
加拿大政府还采购了疫苗生产和包装所需的设备和用品,以及注射器、针头和酒精拭子等接种设备。
杜鲁多还宣布,加拿大将向新冠肺炎疫苗公平分配计划(COVAX)提供4.4亿元资金,这是一项由世界衞生组织等机构共同领导的全球采购计划,旨在确保贫穷国家能公平、公正和及时地获得疫苗。
杜鲁多说,仅由任何一个国家都无法单独解决这种流行病,因为需要在全球所有地方消除这种病毒。
不过,美国不在COVAX名单上。
杜鲁多说,有190个国家加入这一国际联盟,有的是捐助国,有的是受援国,这一事实表明,全世界正团结在一起。
V05
中国普通人年底可以接种新冠疫苗
【加拿大都市网】新冠肺炎疫情当前仍在全球大流行,中国目前已有11款疫苗进入临床试验阶段。什么时候能打上疫苗?同时接种新冠和流感疫苗会冲突吗?新冠病毒变异疫苗还有效吗?人民网将有关新冠疫苗接种的问题图示解答:
中国疫苗世界领先 阿联酋卫生部长接种 钟南山再表态…
【加拿大都市网】9月24日,在第十三届中国生物产业大会上,中国院士钟南山表示,今冬明春新冠肺炎疫情可能继续存在或发展。他介绍,完成大规模接种疫苗需要1至2年的时间。目前,中国与40多个国家保持合作,并已经获批在巴西、俄罗斯等国家开展 III期临床试验,4款疫苗已与国际合作进入 III期临床试验。
疫苗成为恢复全球正常生活秩序的最大希望,中国目前在全球研发疫苗竞赛中处于领先,八支已进入临牀试验最后阶段的候选疫苗,四支是中国产品,比其他国家都多。中国生物研制的两款新冠灭活疫苗已接种数十万人次,据称无一例不良反应,且零感染。相比之下,美国声称只会在满足本国需求后分享疫苗;英国阿斯利康公司疫苗受试者则出现不良反应,暂停疫苗临牀试验。
中国在全球研发新冠肺炎疫苗竞赛中领先,力推“疫苗外交”,塑造国际形象!据悉,中国已与菲律宾、印尼、巴基斯坦、孟加拉等多国展开疫苗合作,阿联酋紧急批准使用中国疫苗,卫生部长更亲身接种疫苗。
目前,中国已与菲律宾、印尼、巴基斯坦、孟加拉等多个国家展开新冠肺炎疫苗合作。阿联酋日前宣布,已紧急批准使用中国国药的新冠疫苗,接种对象是面临感染风险最大的一线医务人员。阿联酋卫生和预防部部长奥瓦伊斯本月十九日更接种了疫苗,并且表示之前的实验证明安全有效。土耳其卫生部部长科贾本月十六日表示,一款由中国研制的新冠疫苗三期临床试验当天在土耳其启动。
疫苗研制超前成为外交利器。总理李克强和外长王毅表示,未来中国生产的疫苗,将优先供给澜沧江──湄公河国家组织成员,非洲兄弟友邦国家更将获无偿提供。
加拿大政府再签7200万剂疫苗订单
(■■联邦与制药公司赛诺菲签新协议,获取7,200万剂新冠状病毒疫苗。 美联社)
联邦政府与法国跨国制药公司赛诺菲(Sanofi)签署了一项新协议,以获取7,200万剂新冠状病毒疫苗。本国迄今已拨款10亿元用于疫苗采购,意味未来至少可获得1.54亿剂疫苗。
采购部长阿南德(Anita Anand)周二还表示,本国准备从吉利德科学公司(Gilead Sciences)和麦基森加拿大公司(McKeeson Canada)的抗病毒药瑞姆昔韦(remdesivir)中,获得多达15万瓶药来治疗该病毒。
本国迄今已拨款10亿元用于疫苗采购,意味未来至少可获得1.54亿剂疫苗。辉瑞、Moderna,强生和Novavax都已跟渥太华签署交易。
潜在疫苗须经3阶段临床试验
为获得批准使用,任何潜在疫苗都必须经过一个成熟的测试过程,包括3个阶段的临床试验。第一阶段和第二阶段的重点,是监测药物是否从人体免疫系统产生所需的反应。第三阶段涉及更多的测试对象,旨在确定候选疫苗是否真的能够阻止病毒感染人体。
赛诺菲及提供佐剂技术的葛兰素史克所合作研发的疫苗,于9月初进入临床试验的第一阶段和第二阶段,共有400名参与者。到2020年底将进入第三阶段试验。
阿南德表示,政府还与英国跨国制药公司阿斯利康(AstraZeneca)进行了会谈。阿斯利康很有机会成为最有希望的疫苗候选人,但该公司9月初试验阶段中发现有志愿者出现副作用而暂时中止。
公司后来宣布恢复试验。有加拿大专家认为,阿斯利康的疫苗最有机会率先成功,试验一度中止代表该公司谨慎并透明的作风,呼吁渥太华务必及早和该公司签订协议。
同时,本国正在敲定与COVAX的合作伙伴关系的细节,COVAX设施是一个国际联盟,旨在推进测试和疫苗。
世卫首席科学家:中国新冠疫苗已被证明有效
【加拿大都市网】世界卫生组织总干事谭德塞表示,结束新冠肺炎大流行和加速实现全球经济复苏的最快方式,是确保所有国家都有人能接种新冠疫苗;世卫组织首席科学家苏米娅·斯瓦米纳坦表示,中国的新冠疫苗研发项目非常活跃,并且一些疫苗在现阶段临床试验中已被证明有效。
在新冠肺炎例行新闻发布会上,世卫首席科学家斯瓦米纳坦表示,中国的一些新冠疫苗已在现阶段临床试验中被证明是有效的。中国的新冠疫苗研发项目非常活跃,已有数个候选疫苗处于临床试验领先(高级)阶段,世卫组织对中国的新冠疫苗很感兴趣,一直在密切关注,一些疫苗在现阶段临床试验中已被证明有效。
特朗普急于批准疫苗 加拿大人吓坏或不敢试
加拿大疫苗专家小组担心,特朗普政府在11月美国总统大选前通过政治努力急于批准疫苗的做法,可能会吓到加拿大人不敢使用。
联邦新冠疫苗工作组联合主席兰利医生(Joanne Langley)和工作组成员伯恩斯坦(Alan Bernstein)表示,他们担心加拿大的“疫苗犹豫”(vaccine hesitancy)现象,人们可能因为担心疫苗的安全性而不敢使用疫苗。
兰利说,当最终发现一种针对新冠的疫苗时,政府和医疗保健专业人员将不得不发起一场强有力的宣传运动来说服反对的人。
但这可能无济于事,因为特朗普曾表示可能于10月推出一款结束疫情的疫苗,令人担忧的是他正加紧进程,以便可以赶上他11月3日的连任机会。
联邦政府疫苗工作组的大约12名医疗专家一直在担心,特朗普这么着急地批准一种疫苗,可能会把人们吓坏了,从而不敢使用这种疫苗。
该工作组的任务是为政府提供建议应该花钱购买哪种疫苗。星岛综合报道
中国11款新冠疫苗临床试验
■中国率先开发新冠疫苗,并投入临测试。
(星岛日报报道)中国疫苗研发领先国际。中国科技部长王志刚昨日在全球科学与生命健康论坛上表示,中国科研人员分别从五条技术路线研发新冠疫苗,目前内地已有十一款疫苗进入临牀试验阶段,其中有四款进入三期临牀试验。军事科学院生物工程研究所所长陈薇透露,下星期在江苏泰州将展开五十五岁以上人群的大规模临牀试验。她还指,病毒变异对疫苗效率的影响微乎其微。
一众抗疫“明星”昨日云集该论坛,陈薇在论坛上表示,其团队联合康希诺公司研制的腺病毒载体疫苗,已有一个疫苗品种上市,还有四个品种处于临牀或临牀前阶段。她还回顾了该疫苗的出炉过程,三期临牀试验已在上月开展,下星期将在泰州展开五十五岁以上人群的大规模临牀试验。此外,陈薇团队还在研究重组新冠抗体,希望为临牀提供可能的特效药。
外界关心病毒变异对疫苗效率的影响,陈薇称,分析过全球六万多条全基因组序列,发现病毒基因最有用的一段,只有一处变异,认为对疫苗的影响微乎其微。她还强调,中国研发的疫苗安全。
中国工程院院士钟南山则通过视频表示,今冬明春,新冠肺炎疫情可能会继续存在或发展。在预防层面,他认为,群体免疫应该通过大规模接种疫苗的方式来实现,但大规模接种疫苗需要大约一至两年的时间,并需要全球各国大合作。
中国疾病控制中心主任高福在论坛发表演讲时透露,目前内地已成立国家新冠病毒中心,将负责收集病毒、基因组序列,进行新冠疫情防控相关的培训、国际合作、协调全国活动、制定国家标准等工作,以便更好地应对新冠肺炎疫情。
特朗普速推新冠疫苗 料明年4月全美可接种
美国总统特朗普周五表示,预计到了明年4月就会制出足够的新冠肺炎疫苗,提供给所有美国人接种,还说首批疫苗将在今年稍后核准后立即分发。
特朗普在白宫举行的记者会上说,美国将在今年底前生产至少1亿剂新冠肺炎疫苗,此后每月将有数亿剂疫苗可用,预计到明年4月份将有足够疫苗供应给每个美国人。
他指出,美国有3款新冠肺炎候选疫苗正处于最后研发及试验阶段,形容这是“历史性的进展”。他又誓言以闪电般速度推出疫苗,他说:“我认为分发速度甚至会比大部分人所想的还快。”对于疫苗研发的时间表,特朗普日前更表示,有可能在10月中旬推出。
但美国医学专家对此则持谨慎态度,国家过敏症和传染病研究所所长福奇、疾病控制及预防中心主任雷德菲尔德等人均认为,疫苗上市初期可能供应十分有限,预计要到明年第二季末或第三季才能普及接种。
对于与医学专家的预期不同,特朗普指出,新冠疫苗研制已处最后阶段,疫苗普及接种的时间将远超专家预期。他还说,一旦获批,美国政府将立即向民众提供疫苗,分发工作将在接到通知后24小时内开始。
从研发周期来看,一款疫苗从开发到获批上市,需要经历多期临床试验、审批,再到大规模生产等过程,通常需要一年半到两年时间。
美国舆论担忧疫苗研制进展得太快,有可能在被证明安全有效之前,就因政治压力而仓促获批上市。
特朗普的竞争对手、民主党总统候选人拜登也对特朗普的疫苗时间表提出质疑,不相信对方会在没有政治干预的情况下推出疫苗。
拜登说:“关于疫苗,我不相信总统。但如果福奇说疫苗是安全的,那我就接受。”
另外,疾控中心上月底疑在华府施压下更改指引,声称即使与患者密切接触,但没有出现病征就无必要接受检测,令专家忧虑这无法找出隐形传播者。疾控中心周五宣布更改回此前的指引,只要与患者密切接触,即使没有出现病征,亦需要接受检测。
根据疾控中心最新的指引,假如民众与患者有持续至少15分钟、在6呎距离内接触,无论有否病征都要接受检测。由于出现患者在无病征或未出现病征下将病毒传播,因此要厘清情况。
指疫苗比口罩更有效 特朗普:美国年底最少有1亿疫苗
在新冠肺炎疫症期间经常批评科学界的美国总统特朗普,周三又公然与疾病预防及控制中心主任雷德菲尔德打对台,扬言美国可能在今年年底或之前,分发最少1亿剂新冠肺炎疫苗。数小时前,雷德菲尔德出席国会听证会时透露,疫苗可能在明年中或稍迟的时间才会有大量供应。特朗普反驳雷德菲尔德的说法,指雷德菲尔德“搞乱了”。同一天,民主党总统候选人拜登听取了有关疫苗研发工作的汇报,表明:“我只信任疫苗和科学家,不信任特朗普。”
特朗普向记者发表谈话时,提到雷德菲尔德出席参议院听证会时所提供的有关疫苗的资料。特朗普说:“不,但我认为他说出那番话时,犯了错误。那些是不正确的资料。我认为他只是误解了问题。可能是。”
雷德菲尔德在听证会上称,疫苗要等到2021年第2季末或第3季,才会有普遍供应。他又表示,戴口罩预防感染新冠肺炎病毒,比注射潜在疫苗更加有效。
他指出:“疫苗可能最快于今年11月或12月作好准备,但初期只会有限度供应,让最高危的人注射。若要我们有足够的人接种,我认为要等多6个月至9个月。”
特朗普回应记者追问时,很明显不满意雷德菲尔德的说法,指雷德菲尔德“搞乱了”,又指他可能不明白议员所问的问题。特朗普指出,美国最快会于今年年底或之前,便会有最少1亿剂疫苗供应。他又反驳雷德菲尔德的口罩论,重申戴口罩会产生许多问题。
不过,特朗普随即补充说,他仍然信任雷德菲尔德和他的工作。
另一方面,拜登周三在他的家乡特拉华州发表讲话,批评特朗普应对疫情毫不认真。他谓:“总统的首要责任是保护美国人民,但他没有,完全不合符资格。让我说清楚:我信任疫苗、信任科学家,但我不信任特朗普。在这一刻,美国公众也不可以(信任特朗普)。”
拜登说,如果明天有疫苗供应,他会马上去注射,但他警告特朗普政府,不要急于在11月3日全国大选投票日之前,推出未测试完成的疫苗。任何疫苗都必须严格达到安全标准。
约翰‧霍普金斯大学最新数据显示,美国全国至今共有接近663万宗确诊个案,超过19.6万人死亡。
【牛津疫苗】再有接种者不适发烧发冷 暂停新一剂注射
英国药厂阿斯利康(AstraZeneca)与牛津大学研发的新冠病毒疫苗原定明年面世,但再有暗涌,英媒周四报道,另有一名接种人士在注射疫苗14小时后发烧、头痛,甚至全身乏力,并持续多天。尽管如此,有其他志愿者仍然乐于及渴望接种新一剂疫苗。
较早时有接种人士疑似出现脊髓炎副作用而暂停测试,英国《每日邮报》报道,再发现有一名5月时接种首剂疫苗的志愿者,他于疫苗注射后翌日凌晨2时在睡梦中惊醒,并感到身体发热又发冷,体温升至摄氏39度以上,服用退烧药后仍无法退烧;更感到极度不适、四肢乏力,只能睡一整日。
虽然他在第3日已退烧,严重症状已没有出现,但副作用仍然持续。
按照要求,接种人士需每周在网上登记健康状况,方便研究人员跟进。他原定于周一接受加强剂量疫苗注射,惟疫苗项目经理在前一天以电邮通知取消,称需要审慎调查每位接种人士的病征,并把个案交由独立安全调查委员会及监管机构调查。
另一名志愿者35岁男自由身记者萨默斯(Jack Sommers)仍然相信测试是安全,表示对暂停感到失望,称大家都急不可待希望研发出疫苗。他又认为如果有大问题应该他现在已经倒下,所以不担心接种第二剂疫苗。
他认为,在18000多名参与测试志愿者中,数据上无可避免有至少一人有些到不适。他认为计划有牛津大学、药厂、英国政府支援,在动物上进行过多次测试,他希望亲身粉碎网络上有关新冠病毒疫苗的阴谋论,又觉得参与者应该本身理解会有风险。